Les plénières de la cuvée 2024 de la CROI ont été particulièrement riches et originales. De plus elles constituent des ouvertures sur le reste du programme et permettent souvent de disposer d’une synthèse de ce qu’il y a de nouveau sur un thème sans pour autant suivre les sessions plus détaillées. Les sujets : vaccinologie, transmission mère-enfants et criminalisation des LGBTQI+ étaient au programme de la plénière d’ouverture dimanche soir. Puis nouveautés sur les vaccins et papillomavirus le lundi, du fondamental sur la capside virale et tuberculose le mardi et enfin, la fin des formulations orales de médicaments et de la nouveauté en matière de tests de dépistage le dernier jour. Un programme particulièrement varié.

La plénière de mardi
La première présentation de ce mardi a de quoi réveiller les neurones des congressistes. C’est de la recherche fondamentale. Eric O. Freed du National Cancer Institute nous propose : « HIV Assembly, Maturation Inhibitors, and Drug Resistance ». Nous sommes plongés à l’échelle cellulaire pour observer la production de nouveaux virus par une cellule infectée par le VIH.
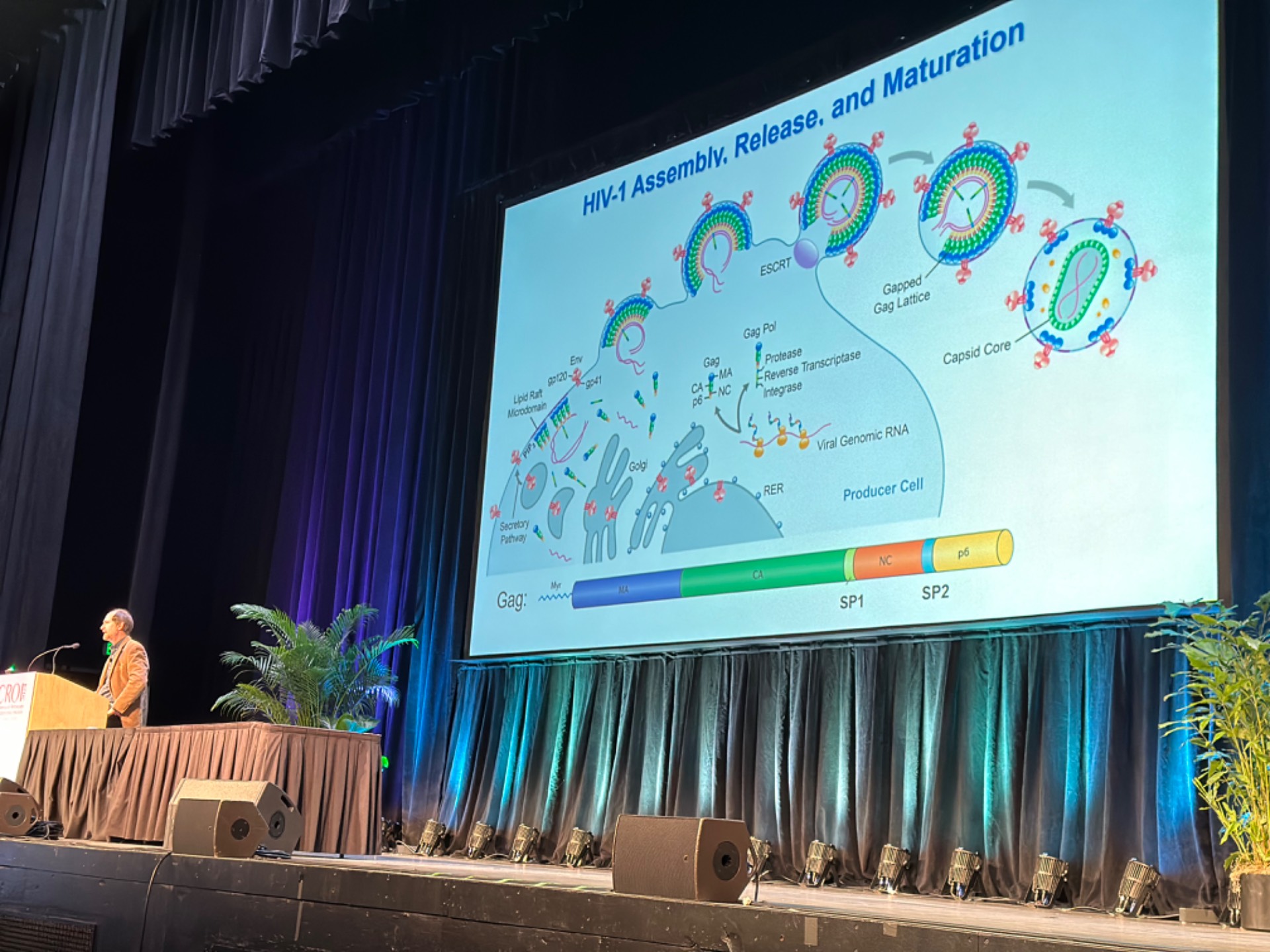
L’assemblage des particules du VIH-1 est piloté par le précurseur polyprotéique viral Gag, qui initie l’assemblage en formant des copies protéiques de Gag immatures au niveau du feuillet interne de la membrane plasmique cellulaire infectée. Une fois l’assemblage des particules immatures et le bourgeonnement du virus terminés, la protéase virale clive le précurseur Gag en un certain nombre de sites, ce qui libère les différentes composantes qui vont permettre de générer la matrice (MA) des protéines Gag matures, la capside (CA), la nucléocapside (NC), la protéine p6 et deux petits peptides espaceurs SP1 et SP1.
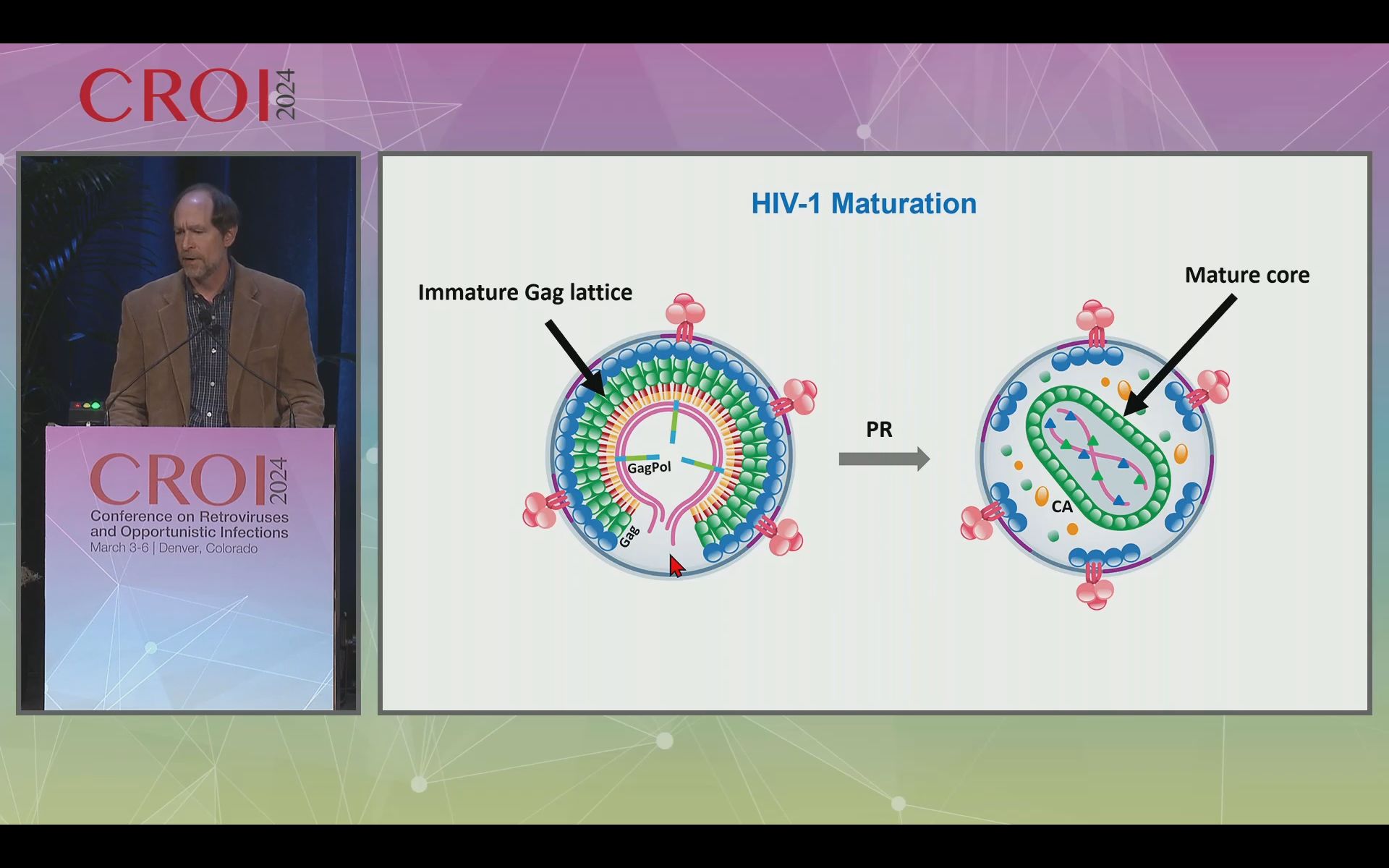
Le clivage de Gag par PR déclenche une transformation morphologique du virion naissant libéré (connu sous le nom de maturation) au cours de laquelle la protéine CA nouvellement libérée s’assemble pour former la capside virale, dans laquelle sont empaquetés le génome de l’ARN viral et les enzymes virales, transcriptase inverse (RT) et intégrase (IN). Les recherches de l’orateur et celui d’autres chercheurs ont démontré que la stabilité fine du réseau Gag immature est essentielle à l’assemblage des particules et à leur maturation ultérieure De même, une bonne stabilité de la capside est essentielle pour le bon déroulement des événements qui se produiront lors de l’entrée du virus ainsi formé dans une cellule à infecter. La stabilité des réseaux Gag immatures et matures est modulée par une protéine cellulaire, inositol hexakisphosphate (IP6).
Deux classes d’inhibiteurs du VIH-1 – les inhibiteurs de maturation et les inhibiteurs de capside (y compris le médicament lénacapavir – agissent en faisant basculer l’équilibre stabilité/instabilité du réseau Gag immature et de la capside mature, respectivement. Ainsi, élucider les déterminants de la stabilité du complexe Gag est crucial à la fois pour comprendre la réplication du VIH-1 mais aussi pour faire avancer les efforts de découverte de médicaments ciblant l’assemblage, la maturation ou les événements post-entrée qui dépendent de la capside, y compris l’importation dans le noyau cellulaire.
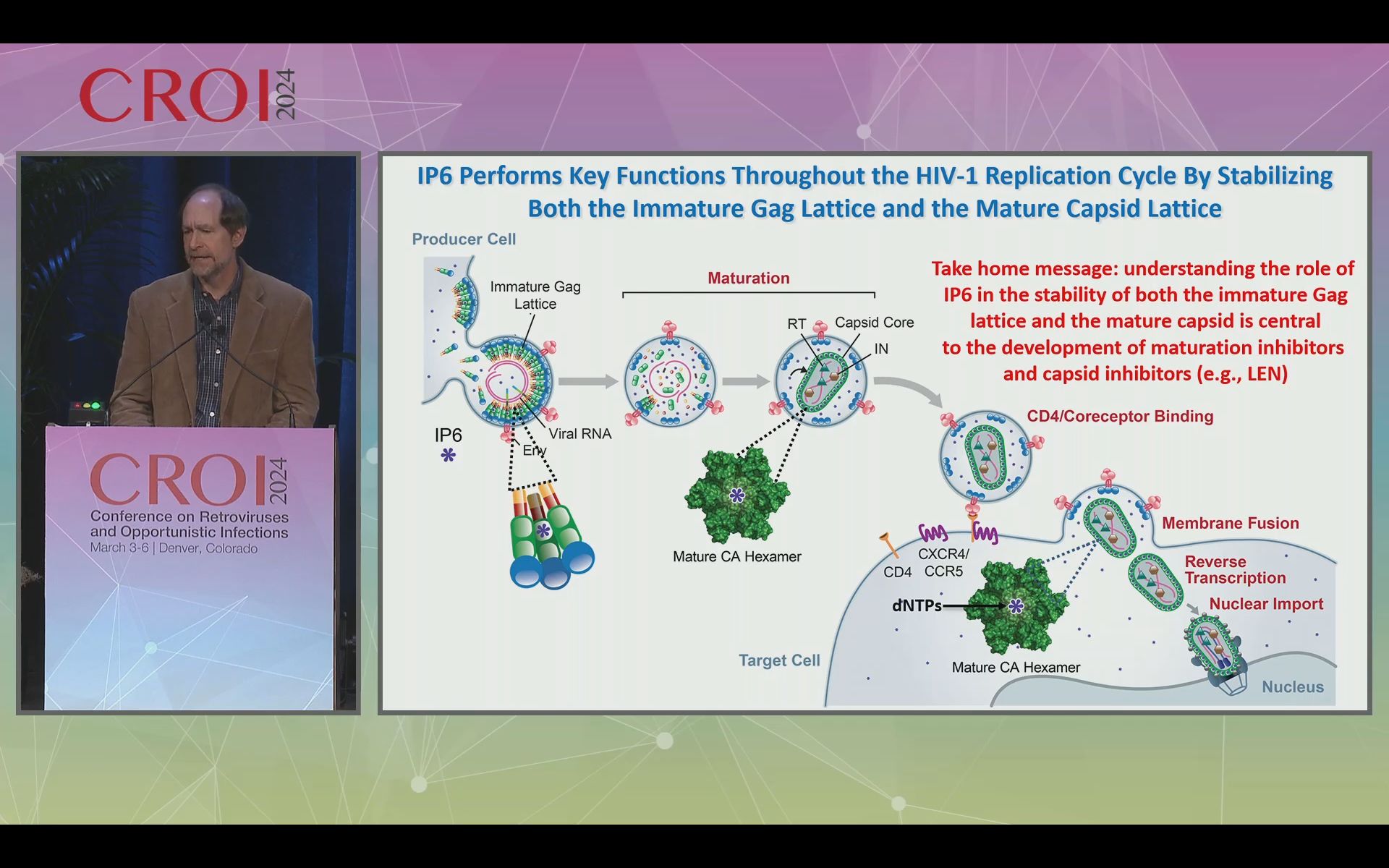
Dans une autre piste de recherche, les travaux de l’orateur ont montré que la composition lipidique du virion du VIH-1 joue un rôle clé dans la maturation du VIH-1, car la perturbation de la biosynthèse cellulaire des lipides, l’enzyme sphingomyélinase neutre 2 (nSMase2), bloque le traitement de Gag, et donc bloque la maturation et la réplication du virus.
Toutes les études sur les sélections de résistance aux médicaments antirétroviraux dont il est question ici et les expériences d’évolution forcée ont fourni des informations clés pour comprendre les mécanismes fondamentaux de la réplication virale.
Dans la deuxième plénière du jour, Vidya Mave du Center for Infectious Diseases in India nous parle de tuberculose dans sa présentation : « Accelerating Tuberculosis Elimination: Short-Course Prevention and Treatment ».
Dans la deuxième plénière du jour, Vidya Mave du Center for Infectious Diseases in India nous parle de tuberculose dans sa présentation : « Accelerating Tuberculosis Elimination: Short-Course Prevention and Treatment ».
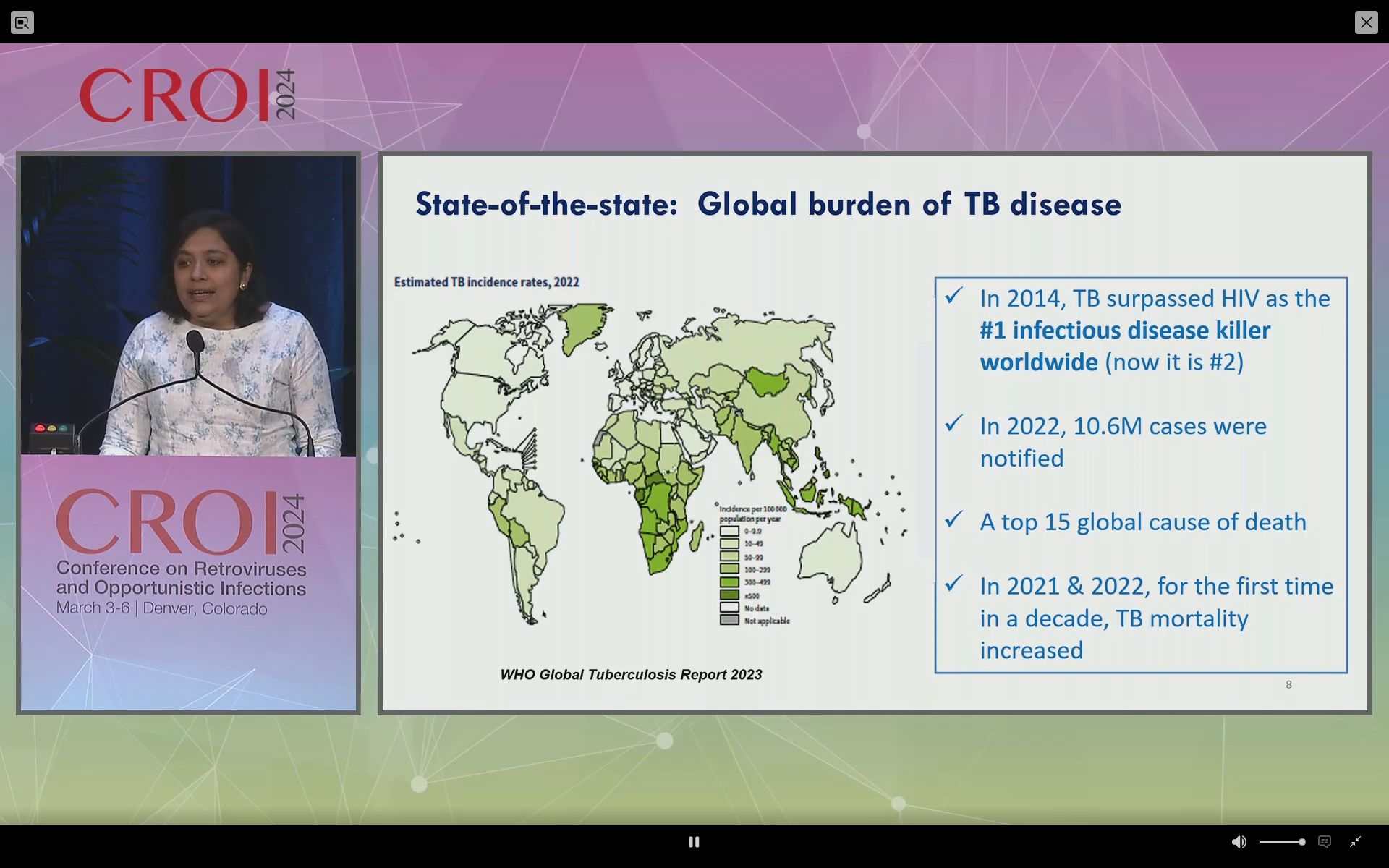
La tuberculose (TB) est l’une des principales causes de morbidité et de mortalité dues à une maladie infectieuse, chez les patients avec et sans VIH, dans le monde. Malgré un traitement antituberculeux (ATT) gratuit de 6 mois, les taux de guérison de la tuberculose ont été sous-optimaux en raison d’une observance inadéquate du traitement antituberculeux, entraînant un risque plus élevé d’échec, de rechute ou de résistance acquise aux médicaments, en particulier dans le contexte du VIH. Des développements récents en recherche ont démontré que les schémas thérapeutiques ATT très puissants peuvent permettre de raccourcir la durée du traitement antituberculeux, tant pour la tuberculose pharmaco-sensible que pour la tuberculose résistante aux médicaments, chez les adultes, les adolescents et les enfants. En outre, un traitement préventif raccourci contre la tuberculose contenant des rifamycines et de l’isoniazide très puissants est aussi efficace que la prophylaxie traditionnelle à l’isoniazide de 6 à 9 mois parmi les populations à risque. En outre, de nouvelles données montrent que les schémas thérapeutiques et de prévention raccourcis de la tuberculose peuvent réduire l’impact des interactions médicamenteuses avec les antirétroviraux. La présentation de l’oratrice donne essentiellement les résultats des recherches récentes sur la prévention et le traitement de la tuberculose en traitement court, dont plusieurs ont désormais inspiré les lignes directrices de l’OMS. Finalement, elle évoque les premiers résultats des études d’injectables à longue durée d’action pour le traitement de la tuberculose.
La plénière de mercredi
Dernier jour de cette CROI 2024. La plénière du matin est placée sous le signe de la nouveauté, que ce soit en matière de traitements antirétroviraux ou à propos des techniques de dépistage. C’est Charles W. Flexner de Johns Hopkins University, Baltimore qui ouvre la session avec une présentation titrée « The End of Oral? How Long-Acting Formulations Are Changing the Management of Infectious Diseases ».
Pourquoi les traitements oraux échouent à contrôler l’épidémie de VIH ? C’est par cette question que l’orateur entame son propos. Il explique. Malgré les formulations quasi parfaites de pilules combinées orales pour des traitements antirétroviraux quotidiens, la persistance des traitements est faible, les échecs sont élevés et le manque d’observance est commun. Les formulations « long-acting » ou à action prolongée, devraient apporter la meilleure réponse à ces constats. C’est bien ce que montrent les expérimentations du cabotégravir injecté toutes les 8 semaines qui fait mieux que le traitement oral. D’ailleurs les enquêtes montrent une meilleure acceptation de ce type de formulation chez les personnes vivant avec le VIH.

Comment est obtenue une formulation à action prolongée ? Pour ce qui est du cabotégravir et de la rilpivirine, la substance active a été produite sous forme de nanocristal en suspension dans un liquide. Ces nanocristaux facilitent la dissolution. Ils sont de taille variable, ce qui assure une diffusion à durée variable selon la taille et permet ainsi une diffusion lente, continue et à longue durée. Mais cette méthode n’est utilisable que pour des molécules hydrophiles, ce qui explique qu’il n’y a pas d’inhibiteurs nucléosidiques en formulation d’action prolongée. C’est pourquoi d’autres méthodes sont à l’étude. Celle de produire une prodrogue a été testée avec l’emtricitabine. Une autre solution, la production de nanoparticules lipidiques est testée sur un composé lamvudine, tenofovir, dolutegravir. Ce dispositif permet d’obtenir une diffusion prolongée sur un mois. Le bictegravir, lui aussi, fait l’objet de tentative de ce genre. Également testé, une forme de al lamivudine, produite sous forme de polymère peptidique. Cette formulation permet d’obtenir une diffusion sur plus de 30 jours chez la souris.
D’autres médicaments bénéficient aussi de ces recherches. Ainsi, un anti-tuberculose, la bedaquiline, a été réalisé sous forme d’un produit qui permet une diffusion pour une durée d’action de 175 jours. D’autres produits comme la rifapentine et la diarylquinolone sont actuellement testés sur des modèles souris pour une diffusion mensuelle. D’autres techniques sont également utilisées. Il est ainsi des implants. Une étude sur un implant diffusant du TAF a été montée, l’étude CAPRISA 018 [sur laquelle nous reviendrons plus tard, ndlr] qui a montré un intérêt sur la diffusion du produit mais qui s’est heurté à des difficultés au niveau des implants.
L’hépatite C bénéficie aussi de ces recherches. Deux antiviraux, le glecaprevir et le pibrentasvir sont en cours de développement en nano suspension, avec des concentrations efficaces pendant 2 mois. Ce que visent ces recherches, c’est d’obtenir des formulations qui permettraient de traiter une hépatite C en une fois, une administration de produit en cas de test positif permettrait de traiter immédiatement la maladie.
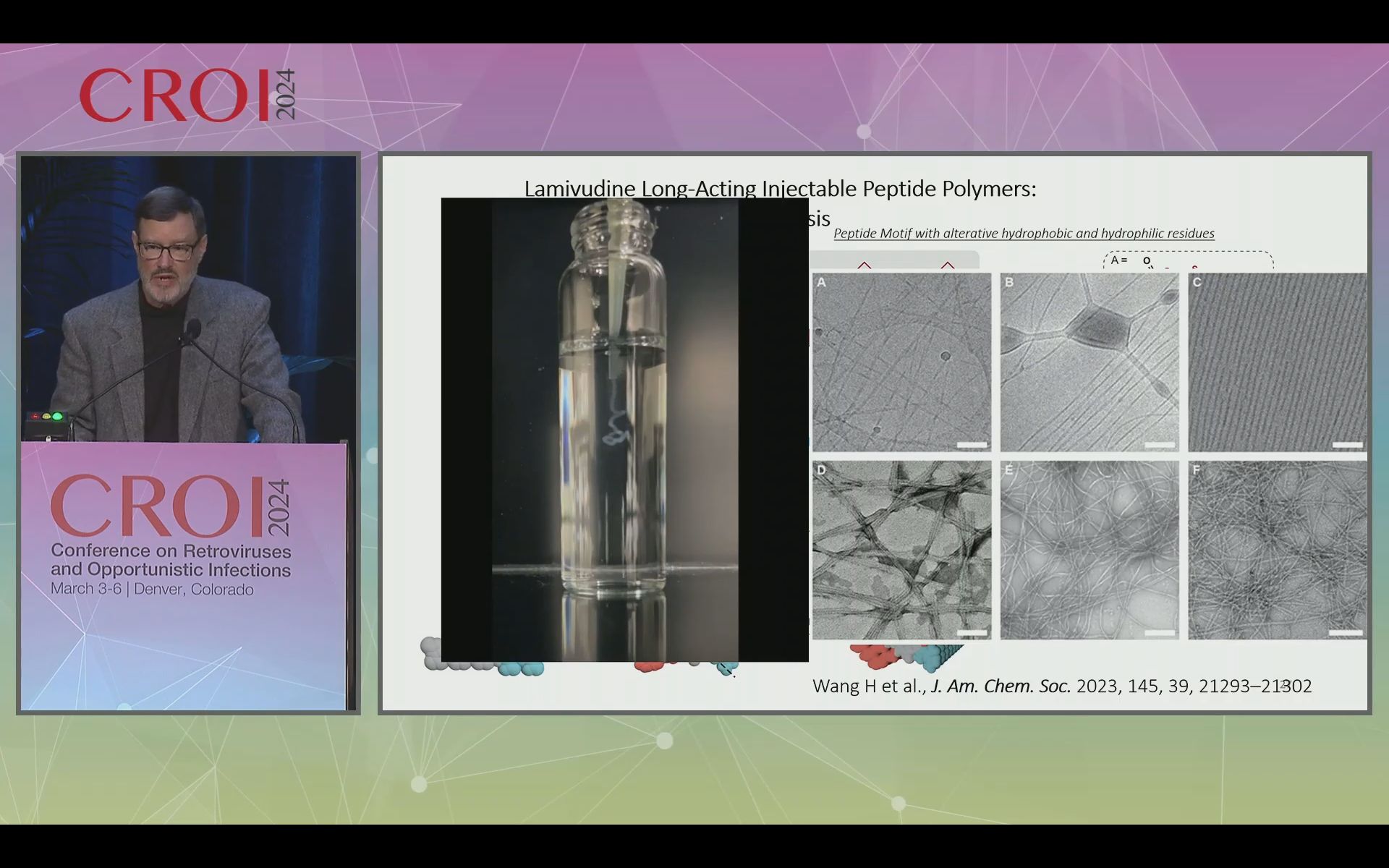
La particularité des formulations à diffusion lente et à longue durée d’action par rapport à la formulation orale est de changer les paramètres de la pharmacocinétique. Traditionnellement, la concentration des molécules est contrôlée par leur vitesse d’élimination, rénale ou hépatite. Avec les dispositifs à diffusion lente, la concentration est obtenue par la vitesse de diffusion du produit à partir de son implantation. Pour bien se figurer la chose, une modélisation a été réalisée avec le lopinavir, habituellement formulé en pilule orale associée avec un booster, le ritonavir, qui ralentit son élimination hépatique. Formulé en injection à longue durée d’action le lopinavir pourrait être administré sans ce booster.
En conclusion, l’orateur est revenu sur l’accès aux traitements dans les pays du monde. Il a insisté en particulier sur l’estimation de 84 000 décès annuels d’enfants dus au sida très majoritairement dans les pays à faibles ressources. Cela est le résultat notamment de l’insuffisance de formulation pédiatriques. Les essais de ces nouvelles formulations capables d’améliorer la vie des personnes vivant avec le VIH se fait actuellement et comme toujours, dans les pays riches. Si l’on veut tenir compte du passé, il est indispensable de développer les formulations à longue durée d’action en parallèle dans les pays du nord et du sud, surtout là où l’épidémie est la plus importante. Les personnes n’échouent pas avec les médicaments, les médicaments échouent chez les gens.

La dernière présentation en plénière de cette CROI 2024 est consacrée à un sujet qui nous semble banal mais qui a toute son importance comme nous le rappelle Nitika P. Pai de l’université McGill à Montréal, dans sa présentation : « Diagnostics 4.0: The Future of Diagnostics for HIV and Related Infections », parce qu’il constitue l’outil essentiel du diagnostic et de la prévention, le dépistage.
L’importance du dépistage VIH n’est plus à démontrer. Pour atteindre l’objectif voulu par l’ONUSIDA des 95-95-95 il y a encore une marge de progression puisque nous sommes en gros aujourd’hui à 86-89-93. On le voit bien, cette marge de progression est surtout celle de dépister l’épidémie cachée. 14% de personnes vivant avec le VIH ignorent leur statut. Et on sait bien que ce sont ces personnes qui alimentent l’épidémie puisque les études ont montré que la transmission est sept fois plus fréquente chez les personnes qui ignorent leur statut que celles qui le connaissent. Ces personnes constituent la cible principale du dépistage.
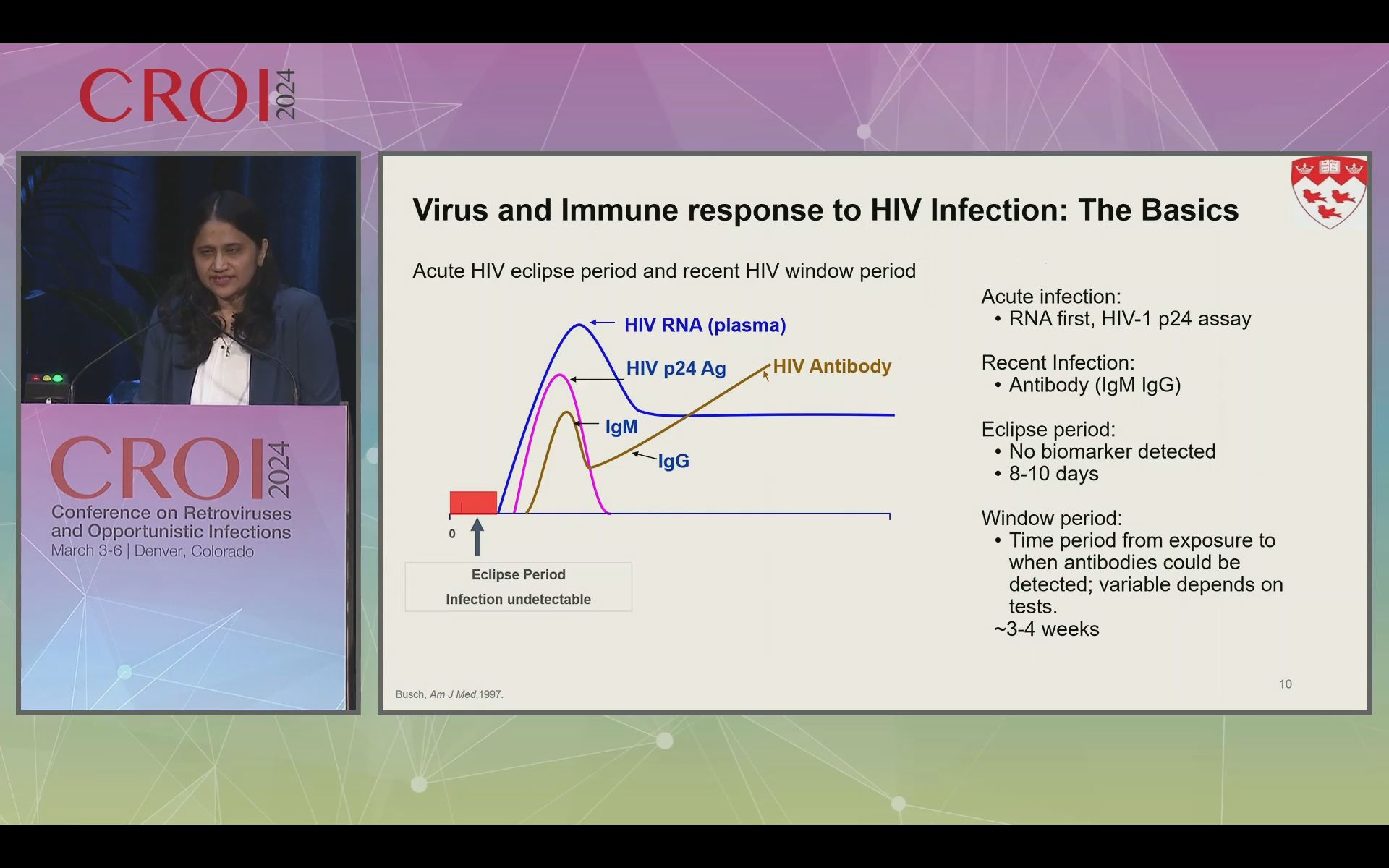
Rappelons quelques bases pour bien comprendre l’enjeu. A partir de l’acquisition du virus, quel que soit le mode de transmission, il se passe une période éclipse où rien n’est détectable d’environ 8 à 10 jours. Puis apparaissent les premiers marqueurs mesurables, l’ARN viral en premier puis l’antigène p-24 du virus. C’est la période d’infection aigue. Ensuite apparaissent les anticorps anti-VIH. Entre l’exposition au virus et l’apparition des anticorps, s’écoule environ 3 à 4 semaines, c’est la fenêtre de séroconversion. La cible des interventions de prévention est donc de réduire autant que possible le délai entre exposition et test de dépistage. Les tests utilisés doivent avoir la meilleure sensibilité possible pour détecter le plus précocement l’infection, mais encore faut-il que le délai entre exposition et présentation à un test soit court. Tout l’enjeu est là.

La technologie des tests n’a fait qu’évoluer depuis le premier test. Elle est aujourd’hui adaptée aux contextes d’utilisation. Aux laboratoires de biologie, les plates-formes capables d’analyser de multiples échantillons dans des automates avec des techniques d’analyse moléculaires, d’amplification génomique ou des dispositifs d’analyse connectés. Au dépistage sur le terrain, les tests rapides (les TROD) capables de rendre un résultat en peu de temps et peu de manipulation mais qui sont un peu moins sensibles que les solutions de laboratoire. Dans ce contexte, de plus en plus de tests multiples sont développés, combinant VIH, hépatites ou IST. A la maison, deux technologies sont employées, l’autotest et l’auto-prélèvement. Le premier rend un résultat immédiat avec un peu moins de fiabilité, l’autre permet une analyse en laboratoire mais rend un résultat moins vite.
De 1985 à 2024, l’évolution des dispositifs ont rendu les tests de dépistage de plus en plus adaptés aux contextes d’utilisation et de plus en plus précis. Cette évolution a permis aussi de faire évoluer les exigences de résultats. Le test ELISA a permis au départ de dépister les nouveaux cas d’infection. Avec le western blot, la précision du diagnostic s’est trouvée renforcée. Les tests combinés et l’amplification de l’ARN ont permis de développer de nouvelles stratégies de dépistage ciblées. Les tests rapides ont rapproché le dépistage des actions de prévention de terrain où le conseil et le soin sont présents. Les nouvelles technologies augmentent la précision, la rapidité et la décision diagnostique.
Avec le développement des autotests apparus en 2012, le champ de l’accès au dépistage s’est élargi. De nouvelles recommandation de l’OMS ont soutenu l’utilisation des autotests en 2016. Aujourd’hui, 98 pays dans le monde ont des règlementations en faveur de l’utilisation de ces tests et dans 52 pays ils sont utilisés en routine. L’ONUSIDA préconise son usage pour atteindre le premier « 95 » de sa cible en 2030. Son développement et surtout son accessibilité sont des clés des programmes de dépistage. L’autotest a été démontré comme un dispositif coût-efficace, pratique, capable d’augmenter la fréquence de test et la proposition de test au partenaire. Il est facile d’en organiser la distribution massive et peut être rendu accessible par de nombreux moyens, des distributeurs à la vente en ligne. Aux Etats-Unis, une campagne de distribution à large échelle a montré son efficacité, et l’objectif du CDC est la distribution de plus d’un million de tests dans les 5 années à venir. Autre exemple innovant, en Afrique du Sud, la distribution d’autotests associée à une application permettant l’aide à l’utilisation, à l’interprétation du résultat et au lien avec les centres de soins a obtenu un succès dans les populations des townships.

Mais les nouvelles technologies ont envahi le terrain du dépistage. Des dispositifs de plus en plus sophistiqués autorisent aujourd’hui le rapprochement des techniques de pointe de l’analyse biologique des lieux de soins (technologies microfluidiques et nanofluidiques). Le next-generation sequencing permet la détection de mutations de l’ADN et l’ARN, la détection de variants en un temps record, ce qui rend accessible les analyses d’évolution des populations virales, la détection précoce de résistance aux traitements, permettant une meilleure adaptation des traitements et plus rapide. Et puis il y a aussi la génomique, la métabolomique, la métagénomique, l’analyse multi-omique, le CRISPR… Des techniques extrêmement pointues dont il faudra quand même surveiller l’accessibilité réelle compte tenu de leur coût.
Et bien entendu, l’intelligence artificielle vient s’ajouter à toute cette technologie, nous faisant entrer dans le monde du diagnostic 4.0 en ajoutant aux techniques d’analyse une couche d’interprétation basée sur des algorithmes et de l’apprentissage machine. L’idée est là aussi de donner un accès par application sur smartphone pour encourager les pratiques de santé, faciliter le lien des personnes avec le soin, améliorer la qualité des autotests, documenter les résultats. Et mieux encore, l’apprentissage machine est capable d’améliorer la qualité des algorithmes de prédiction en matière de progressions de la maladie, aider aux décisions cliniques, prédire les risques de rupture de soin des malades. Mais aussi, en aide à la prévention, les techniques d’IA en développement pourraient estimer le risque de séroconversion ou de besoin de PrEP en appui aux décisions sur les lieux de soins, voire prédire le statut VIH à travers l’analyse de bases de données, âge, sexe, historique IST et médical, ou en identifiant les paramètres socioéconomiques. Encore une fois, le VIH est leader dans le progrès en matière de diagnostic.
Tous nos comptes-rendus sont dans les pages à suivre :
- CROI 2024 à Denver
- CROI 2024, les plénières – première partie
- CROI 2024, les plénières – deuxième partie
- CROI 2024, morceaux choisis
Sources
Tout le contenu de la CROI 2024 est en ligne à partir d’avril là : https://www.croiwebcasts.org/
