Au cours de la 10e conférence de l’IAS sur la recherche VIH qui s’est tenue à Mexico du 21 au 24 juillet 2019, beaucoup de choses ont été partagées sur les techniques de dépistage. En particulier, depuis l’avènement de la PrEP dont le suivi implique un recours régulier et fréquent au dépistage, de nouvelles questions se posent.
Dans une présentation très complète et détaillée, Bernard M Branson (USA, ex-CDC, Gilead Sciences) Nous explique de quoi sont faits les différents tests de dépistage du VIH et ce qu’on peut en attendre. Sa présentation aborde aussi ces questions nouvelles qui peuvent se poser dans le contexte de la PrEP, c’est-à-dire, en quoi la prise d’antirétroviraux influence le résultat des tests alors que, précisément, dans le contexte de PrEP, les tests de dépistage sont rapprochés et critiques.
C’est justement ce contexte de dépistage à l’époque de la PrEP que Jean-Michel Molina a voulu explorer. Il nous présente bon nombre de résultats et de questions liées au risque de contamination et au dépistage du VIH dans le contexte de l’utilisation de la PrEP.
Au cours de cette cession, il a aussi été question de communication sur la prévention et le dépistage en contexte de PrEP en Afrique du Sud par Ntando Yola ainsi que de la question des résistances du VIH aux antirétroviraux dans le contexte de la PrEP, un point présenté par le Dr Kuritzkes.

De quoi sont faits les tests de dépistage du VIH ? – Bernard M Branson
Le principe général des tests ELISA est de détecter la présence d’anticorps dirigés contre l’agent pathogène que l’on veut pister, ici, le VIH. Depuis le premier test, le principe est de détecter la présence d’anticorps IgG dirigés contre le VIH. Au fil du temps les techniques ont évolué, rendant les tests plus sensibles (moins de risque de faux négatifs) et plus spécifiques (moins de risque de faux positifs). Les tests de la 3e génération détectent en plus les anticorps IgM et ceux de la quatrième génération ajoutent à cela la détection d’un antigène, la protéine p24 du virus.
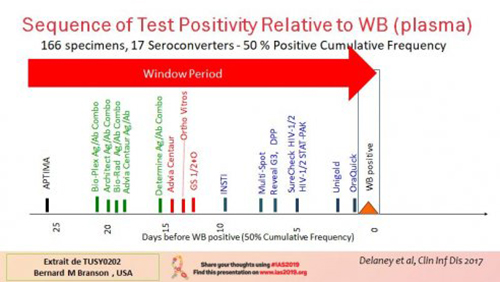
À noter, dans cette vue, les tests à usage unique (utilisés pour les TROD) sont en bleu. Ces temps de délai de détection dépendent avant tout des méthodes utilisées. A partir de la contamination, les délais médians de détection de ces différentes méthodes s’échelonnent de 17,8 jours (tests Ag/Ab sur plasma) à 33,4 jours tandis que le Western Blot est à 36,5 jours. Mais dans la fenêtre de détection, ce qui doit être considéré comme le délai de sûreté pour considérer un résultat positif, ce n’est pas le résultat médian mais celui de 99% des mesures, ce qui devient 44,3 jours à 58,2 jours tandis que le Western Blot est à 64,8 jours (voir tableau de résultat ci-dessous).

À partir de ces mesures, les autorités sanitaires préconisent un délai de sécurité de 45 jours pour les tests Ag/Ab sur plasma (dits de 4e génération) et de 90 jours pour les autres méthodes. C’est ce délai de sécurité qui est annoncé aux personnes qui se font dépister.
Le contexte récent de l’utilisation d’antirétroviraux en prophylaxie (PrEP) a remis en question ces concepts dans la mesure où la présence d’antirétroviraux chez une personne est susceptible d’influencer les résultats des tests. Les antirétroviraux sont capables de rendre l’ARN VIH non détectable et peuvent modifier les résultats des tests dans le temps. On a ainsi constaté que chez des personnes sous traitement, le test de quatrième génération devenait moins performant que ne l’était celui de troisième génération (qui n’est plus utilisé aujourd’hui). Fort heureusement, de nouvelles méthodes de test comme les tests d’acide nucléique sur sang total permettent aujourd’hui de disposer d’outils de dépistage améliorant la fiabilité et la sensibilité des tests dans un délai plus réduit après la contamination. Ils sont aussi plus faciles d’implémentation puisqu’on les opère à partir de petites machines faciles à installer directement dans les lieux de soins et délivrent un résultat dans un délai très court. Mais il reste encore aux autorités sanitaires à adapter la règlementation existante pour pouvoir généraliser leur usage.
Dépistage et PrEP – Jean-Michel Molina
Bien que le niveau de protection contre l’infection que procure la PrEP soit extrêmement élevé, on constate des contaminations par le VIH chez les usagers de cette technique de prévention. Les causes en sont multiples avec, en premier lieu, un mauvais suivi des consignes de prise de la prophylaxie. C’est ce que l’on a constaté depuis les premiers essais cliniques de la PrEP : ça ne marche que lorsqu’on l’utilise. Dans la phase de suivi de l’essai iPrEx (prophylaxie en continu, quotidienne par Truvada), il avait été observé des cas de contamination en dessous du seuil de 4 comprimés par semaine. La deuxième cause est celle de l’intervention PrEP trop tardive. Autrement dit, les personnes candidates à l’usage de la PrEP étant souvent des personnes dont l’exposition au risque est élevée, il arrive que certains ont accès à la PrEP alors qu’ils viennent juste d’être contaminés. C’est notamment ce qui a été observé dans l’essai IPERGAY où on a vu deux cas de personnes dont le test au démarrage était encore négatif mais qui s’est révélé positif un mois après l’inclusion dans l’essai. L’analyse rétrospective des prélèvements a révélé que si le test Elisa de dépistage de 4e génération était négatif chez eux, on a pu trouver par mesure de la charge virale une faible quantité d’ARN viral. Ce cas s’est retrouvé dans d’autres études. C’est la raison pour laquelle les recommandations en cas de démarrage de la PrEP préconisent une attention particulière au test de départ et recommandent de le répéter un mois après l’initiation de la PrEP.
Ces situations étant claires, il reste celles des contaminations durant l’usage de la PrEP. La première est celle des personnes infectées par un virus présentant des mutations de résistance aux antirétroviraux qui constituent le traitement prophylactique, le ténofovir et l’emtricitabine. Les analyses montrent chez ces personnes des virus présentant les mutations de résistance les plus classiques (M184V ou K65R). Si la première est plus fréquente dans les virus transmis, selon la littérature, mais tout de même à un taux de 5 pour mille, la deuxième est bien moins fréquente, moins de 1 pour mille, mais tout de même suffisamment pour que ce type d’évènement ne puisse pas être considéré comme très rare. De multiples cas ont été relevés et étudiés dans la littérature depuis l’avènement de la PrEP.
- Messages de prévention dans le contexte de la PrEP – Ntando Yola



-
La question des résistances du VIH en contexte de PrEP – Daniel R. Kuritzkes
Le Dr Kuritzkes a présenté un point sur la question des résistances du VIH en contexte de PrEP. Non pas que le sujet devienne critique, mais simplement pour faire un point. En effet, malgré les craintes préalables, l’usage de la PrEP n’a pas donné lieu à des émergences de virus résistants essentiellement parce que la PrEP est une protection particulièrement efficace contre la transmission du VIH. Pour autant quelques questions méritent de s’y arrêter un instant notamment concernant les virus résistants circulant. Rappelons-nous que les médicaments antirétroviraux utilisés pour la PrEP sont les mêmes que ceux utilisés en thérapie chez les personnes vivant avec le VIH. L’émergence de virus résistants dans la population des séropositifs pourrait donc avoir une influence sur l’efficacité de la PrEP dans la population. D’une analyse systématique des 699 personnes ayant participé à l’un de 13 essais cliniques de PrEP et a avoir été contaminé par le VIH, toutes causes confondues, montre que le phénomène de résistance reste tout de même marginal. Il concerne 18 des 77 personnes (23%)qui étaient infectées au moment de leur inclusion dans un essai et 19 des 622 personnes (3%) infectées durant les essais. Les résistances, plus souvent à l’emtricitabine qu’au ténofovir, sont plus fréquentes dans les populations de personnes vivant avec le VIH où le suivi médical est faible, cependant elles augmentent en général après la première ligne de traitement. L’utilisation de PrEP à longue durée de d’action pourrait poser d’autres questions en cas d’arrêt de ces traitements et de persistance des antirétroviraux au-delà de la période considérée comme protectrice. Pour toutes ces raisons, il est nécessaire de poursuivre les observations sur la question des virus résistants en contexte de PrEP.
Archives :
Pour approfondir un sujet, toutes ces sessions sont visibles en webcast à partir du site de l’IAS dédié en recherchant la session désirée (elles sont en anglais, la langue de la conférence).
